Un mini-cerveau comme modèle de laboratoire pour l’étude des maladies à prions
La communauté scientifique est aujourd’hui confrontée à plusieurs défis liés à la recherche sur les maladies à prions. L’un des principals et des plus importants est celui qui est axée sur l’étude du fonctionnement de ces maladies humaines, également connues sous le nom d’Encéphalopathies Spongiformes Transmissibles (EST); nous ne disposons pas de modèles de laboratoire (en éprouvette) qui reproduisent fidèlement la complexité de ces maladies dans leur intégralité.
Il y a quelques jours, nous avons appris que des chercheurs du National Institute de la Santé aux États-Unis (NIH, selon son sigle en anglais) ont mis au point le premier système de cerveau organoïde humain, ou mini-cerveau, pour l’étude des maladies à prions. Ce serait le modèle le plus proche d’un vrai cerveau que nous connaissions à ce jour.
Ces mini-cerveaux sont de minuscules sphères ou boules de cellules cérébrales humaines de très petite taille, comme un petit pois, qui présentent les principales caractéristiques d’un cerveau humain, puisque leur organisation, leur structure et leur signalisation électrique sont similaires à celles du tissu cérébral humain. Les organoïdes, en plus d’être composés de neurones, les principales cellules du système nerveux central (SNC), contiennent également des astrocytes et des oligodendrocytes, d’autres types de cellules nerveuses. Ces derniers peuvent également jouer un rôle important dans le développement de la maladie. Pour toutes ces raisons, ainsi que parce qu’ils peuvent survivre dans un environnement de laboratoire contrôlé pendant des mois, voire des années, ces modèles sont utilisés pour l’étude des maladies neurodégénératives, telles que la maladie d’Alzheimer ou le syndrome de Down.
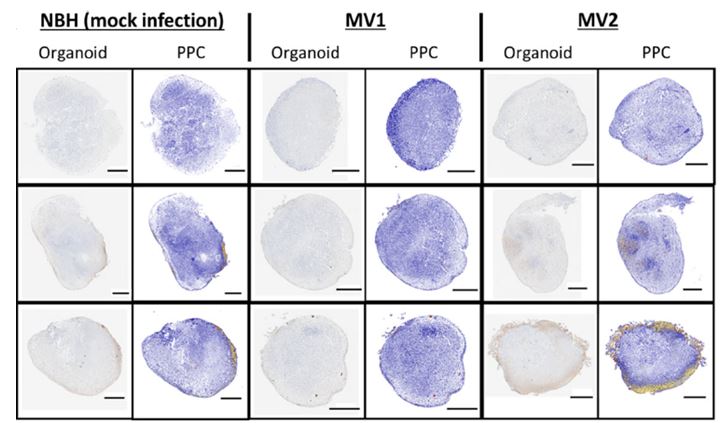
Les auteurs de l’étude, publiée dans la revue scientifique Acta Neuropathologica Communication, ont mis au point ces mini-cerveaux en utilisant des cellules souches pluripotentes inductibles (cellules iPS, selon son sigle en anglais) dérivées de la peau (c’est-à-dire qu’ils ont réussi à convertir des cellules de la peau en cellules du système nerveux). Les scientifiques ont pu infecter ces organoïdes (à l’âge de 5 mois) à l’aide d’échantillons provenant de deux patients présentant deux sous-types de la maladie de Creutzfeldt-Jakob (MCJ) sporadique (sMCJ), MV1 et MV2. Au cours de la recherche, les scientifiques ont surveillé les mini-cerveaux afin de confirmer l’infection et de rechercher des changements dans les paramètres associés à la maladie. Ils ont ainsi pu confirmer la maladie un mois après l’infection des organoïdes et ont décrit les modifications du métabolisme et d’autres paramètres liés à la maladie et à sa progression.
D’autre part, une caractéristique importante de la MCJ est l’hétérogénéité de ses différents sous-types, ce qui complique encore l’étude et la modélisation de cette maladie. Dans cette étude, les auteurs ont observé que les sous-types sCJD MV1 et sCJD MV2 affectent différemment le même type de mini-cerveau. Ils ont observé que les organoïdes infectés par le sous-type MV2 présentaient une activité d’ensemencement, un paramètre lié à la propagation de l’infection, plus élevée que ceux infectés par le sous-type MV1. En revanche, les organoïdes infectés par MV1 présentaient plus de dommages au mini-cerveau que ceux infectés par MV2. Bradley R. Groveman et les autres auteurs de cette étude indiquent que cette nouvelle technologie de système organoïde est encore en cours de développement et pourrait être d’une grande utilité à l’avenir, en aidant à comprendre pourquoi différents sous-types d’une même maladie affectent des zones spécifiques du cerveau et pas d’autres, ainsi qu’en éclairant le mécanisme de propagation des prions entre les cellules.
Enfin et surtout, Groveman et ses collègues espèrent apprendre comment prévenir les dommages cellulaires et restaurer les fonctions cérébrales endommagées par la maladie, même s’ils reconnaissent que ce modèle, bien que prometteur, présente certaines limites. Parmi elles, la grande hétérogénéité des mini-cerveaux, l’absence de vaisseaux sanguins ou l’absence d’autres types de cellules que l’on trouve habituellement dans le cerveau, comme la microglie. Malgré tout, ces nouveaux mini-cerveaux représentent un modèle prometteur pour l’étude des mécanismes de la maladie et, surtout, pour l’essai de futurs traitements potentiels des maladies à prions.
Vous pouvez également le trouver dans : https://asociacioncjd.org/2019/06/18/un-mini-cerebro-como-modelo-de-laboratorio-para-el-estudio-de-las-enfermedades-prionicas/